В сочетании с хирургической терапией радиоактивное золото используется в борьбе с раком. Его особые свойства используются в препаратах для лечения рака, туберкулеза, ревматоидного артрита и дерматологических заболеваний.

Все о золоте (Au): что это такое, химические и физические свойства + интересные факты
Никогда бы не подумал, что существуют люди, которые не знают ценности золота. Оказывается, индейцы Южной Америки называли этот бесполезный, по их мнению, металл. ‘экскременты богов’ и ‘пот солнца’! Они были удивлены шумихой вокруг него. А белые новоприбывшие уверяли туземцев, что те страдают от болезни сердца, которую может вылечить только этот драгоценный металл. Кстати, отчасти это правда. Однако давайте поговорим о свойствах золота более подробно.
Самое распространенное его определение — драгоценный или благородный металл. Но что означает это описание?
Благородство определяется редкостью, долговечностью и привлекательностью. А драгоценность определяется тем, с чем оно вступает в реакцию. Интересно то, что золото не вступает в реакцию ни с одним неметаллическим элементом, включая кислород, что означает, что оно не может вступить в реакцию с течением времени или в суровых условиях.
Физические и химические свойства
Элемент номер 79 в таблице Менделеева, Aurum, не имеет твердости, но обладает высокой плотностью, что объясняет его большой вес. Я предлагаю вам познакомиться с этим металлом поближе — я уверен, что у золота есть много свойств, о которых вы не знали.
Отражающие свойства
Этот металл известен своей способностью отражать инфракрасное и ультрафиолетовое излучение, пропуская при этом большую часть света, поэтому золото широко используется в остеклении небоскребов, при создании визоров для шлемов космонавтов и в приборостроении.
способность к распылению
Да, этот драгоценный металл — мастер распыления. Настолько, что ученые утверждают, что в мировом океане его около 6 000 000 тонн!
Пластичность и ковкость
Это еще два свойства, которые сделали его фаворитом среди ювелиров. Ему можно придать любую форму, он легко сжимается и растягивается, его не нужно ломать, чтобы согнуть. Для производства 100 метров тонкой проволоки для жетонов требуется всего 1 грамм чистого металла.
Пластичность
Одним из важных свойств этого металла является его пластичность. Полупрозрачные чешуйки, обладающие всеми характеристиками типичного драгоценного металла, могут быть сформированы практически при любой температуре, а толщина чешуек составляет от 1 до 0,1 микрометра. Для сравнения, толщина человеческого волоса составляет 80-100 микрометров. Такие листы используются для покрытия предметов интерьера и куполов церквей. Один грамм золота дает лист площадью 0,5 м2.
Электропроводность
С точки зрения электро- и теплопроводности наш главный герой показывает хорошие результаты. Это неплохой проводник, но он уступает серебру и меди.
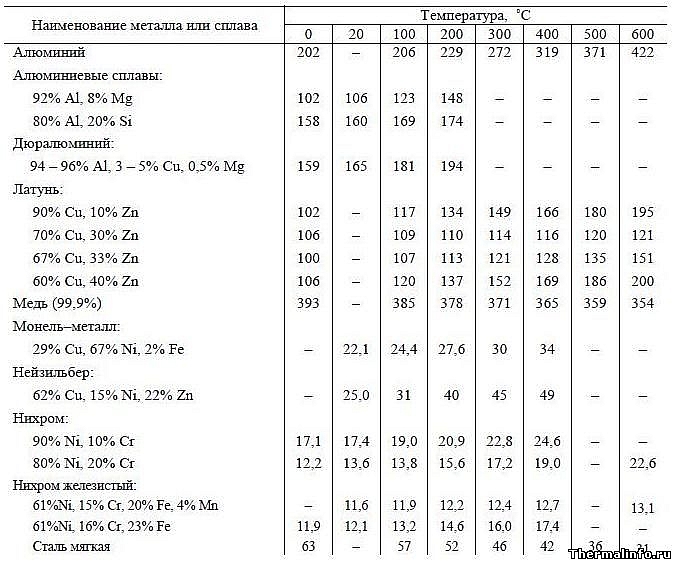
Коэффициенты теплопроводности сплавов алюминия, меди и никеля
Коэффициенты теплопроводности металлов, сплавов алюминия, меди и никеля приведены в таблице в диапазоне температур от 0 до 600°C в пересчете на Вт/(м-град).
Металлы и сплавы: Алюминий, алюминиевые сплавы, дюралюминий, латунь, медь, монель, низильвер, нихром, нихромовое железо, мягкая сталь. Алюминиевые сплавы имеют более высокую теплопроводность, чем латунь и никелевые сплавы.
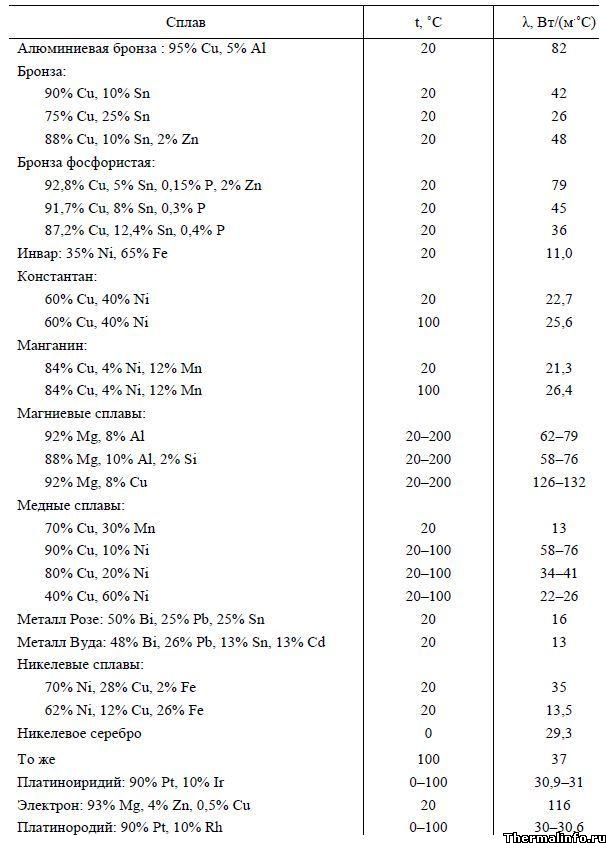
Коэффициенты теплопроводности сплавов
В таблице приведены значения коэффициентов теплопроводности сплавов в диапазоне температур от 20ºC до 200ºC.
Сплавы: алюминиевая бронза, бронза, фосфористая бронза, инвар, константан, марганец, магниевые сплавы, медные сплавы, розовый сплав, деревянный сплав, никелевые сплавы, никелевое серебро, платиновый иридий, электронный сплав, платиновый родий.
Как отличить настоящий желтый металл от подделки
Понимание природы плотности как физической величины поможет нам отличить настоящее золото от подделки. Я подскажу вам, как это сделать.
Au имеет почти самую высокую плотность среди всех драгоценных металлов, кроме платины, а это значит, что почти каждый кусочек золота будет весить больше грамма.
Самый простой способ сделать это — взвесить ваши украшения. Этот метод хорошо работает для небольших ажурных украшений.
Массивные кольца и цепи, браслеты и серьги проверяются по соотношению их веса к объему.
- Точные весы с показателями шкалы до сотых долей грамма;
- мензурка с градуированным объемом. Чем уже мензурка, тем точнее показания. Их можно приобрести в аптеках, а иногда и в аптечных магазинах.
Для примера я попытаюсь определить подлинность (возможно, даже пробу) моего браслета из розового золота:
- Я взвешиваю браслет на весах. Он весит 4,62 грамма.
- Я наливаю воду в мензурку и погружаю в нее браслет. Вода должна полностью покрыть украшение. Браслет вытеснил 0,4 см3 воды. То есть, у меня есть мензурка с объемом CD 0,1 см3, уровень воды поднялся на 4 деления.
- Я вычисляю: 4,62/0,4=11,55 .
- Полученное значение сравниваю с таблицей плотности металлов и таблицей плотности Au (в зависимости от образца).
К полученным значениям приближаются палладий — 12,2, свинец — 11,34, серебро — 10,49. Однако мой браслет имеет приятный розовый оттенок, а это значит, что в нем, скорее всего, есть золото и медь. Из таблицы видно, что плотность моего браслета соответствует 375 пробе — среднему значению для золота, серебра, палладия и меди.
Количество чистого элемента в сплаве определяется по молярной массе золота по формуле M = m/n . Молярная масса Au составляет 196,9665 г/моль.
В моем браслете из 4,62 г и 375 пробы 4,63*0,375=1,74 г золота, 1,74 г/196,9665 г/моль=0,001 моль чистого золота.
Таблица температур плавления тугоплавких металлов и сплавов:
| Название металла. | Температура плавления, o C |
| Лютеций | 1652 |
| Титан | 1668 |
| Торий | 1750 |
| Платина | 1768,3 |
| Цирконий | 1855 |
| Хром | 1907 |
| Ванадий | 1910 |
| Родий | 1964 |
| Технеций | 2157 |
| Хафн | 2233 |
| Рутений | 2334 |
| Иридий | 2466 |
| Ниобий | 2477 |
| Молибден | 2623 |
| Тантал | 3017 |
| Осмий | 3033 |
| Рейн | 3186 |
| Вольфрам | 3422 |
В зависимости от плотности металлы делятся на легкие (с плотностью от 0,53 до 5 г/см³) и тяжелые (с плотностью от 5 до 22,6 г/см³).
Самый легкий металл — литий (плотность 0,53 г/см³). Самый тяжелый металл в настоящее время назвать невозможно, поскольку плотности осмия и иридия — двух самых тяжелых металлов — практически равны (около 22,6 г/см³ — ровно в два раза больше плотности свинца), а рассчитать их точную плотность чрезвычайно сложно: для этого требуется полная очистка металлов, поскольку любые примеси снижают их плотность.
Пластичность:
Большинство металлов пластичны, то есть металлическую проволоку можно согнуть, не сломав. Это происходит благодаря смещению слоев атомов металла без разрыва связей между ними.
Наиболее пластичными металлами являются золото, серебро и медь. Из золота можно изготовить фольгу толщиной 0,003 мм, которая используется для золочения изделий. Однако не все металлы являются ковкими. Цинковая или оловянная проволока хрустит при сгибании; марганец и висмут при деформации почти не гнутся, а сразу ломаются.
Пластичность зависит от чистоты металла. Например, очень чистый хром очень пластичен, но при загрязнении даже небольшими примесями он становится хрупким и твердым. Некоторые металлы, такие как золото, серебро, свинец, алюминий и осмий, могут быть сплавлены вместе, но на это могут уйти десятилетия.
Химические свойства золота
Золото чрезвычайно химически инертно и является единственным металлом, устойчивым к разбавленным или концентрированным кислотам. В нормальных условиях золото не реагирует ни с кислородом, ни с серой. Золото устойчиво к атмосферной коррозии и к различным типам природной воды.
Золото обычно растворимо в водных растворах, содержащих лиганд (который образует комплексы с золотом) и окислитель, но каждый из этих реагентов, взятый отдельно, не способен растворить золото. Например, золото нерастворимо в соляной или азотной кислоте, но легко растворяется в так называемом водном растворе (3:1 HCl + HNO3), образуя HACl4в хромовой кислоте в присутствии хлоридов и бромидов щелочных металлов, в растворах цианидов в присутствии воздуха или перекиси водорода с образованием цианоаурата.
Золото также растворимо в растворах тиосульфатов, тиомочевины, в смесях Кл + I.2при повышенных температурах реагирует с теллуром с образованием AuTe2реагирует со всеми галогенами. Бром наиболее реакционноспособен по отношению к золоту: при комнатной температуре он экзотермически реагирует с золотым порошком, давая Au2Br6. Реакция золота с хлором протекает крайне медленно из-за образования поверхностных соединений. Высокая скорость реакции достигается только при температурах выше 200°C, поскольку при этих температурах хлориды золота сублимируются, в результате чего образуется постоянно открытая чистая поверхность. Продуктом реакции является AuCl3. При восстановлении солей золота дихлоридом олова образуется стабильный коллоидный раствор ярко-красного цвета (‘кассия пурпурная’).
Оксиды золота (AuO2 и Au2О3) можно получить только путем испарения металла в вакууме при высокой температуре. Красновато-коричневый гидроксид Au(OH)3 осаждается при действии сильных щелочей на раствор AuCl3. Соли Au(OH)3 образует со щелочами аураты при растворении в сильных основаниях. Золото реагирует с водородом с образованием гидрида при давлении от 28 до 65-10 8 Па и температуре выше 350°C. Сульфаты MeAu образуются в результате реакции золота с гидросульфидами щелочных металлов при высоких температурах. Известные сульфиды золота Au2S3 и Au2S известны сульфиды золота, но последние являются метастабильными и распадаются на металлическую фазу. Характерной особенностью золота является его выраженная склонность к образованию сложных соединений.
Природное залегание золота
Средняя концентрация золота в земной коре составляет 4,3-10-7 (по данным А.П. Виноградова). По возрастанию концентрации золото выстраивается в следующий ряд природных образований: морская вода, осадочные породы, кислые магматические породы, средние изверженные породы, щелочные и ультраосновные магматические породы, хромитовые базальтоидные породы, гидротермальные руды.
В гидросфере содержание золота составляет 1,0-10-9 %, что более чем на два порядка ниже среднего значения для земной коры. Однако общее количество золота в гидросфере огромно — около 5-6 миллионов тонн. Среднее содержание золота во всех пресноводных видах составляет около 3,0-10-9 %. Содержание золота в морской воде колеблется: в полярных морях 5,0-10-9 %, у берегов Европы 1-3,0-10-7 %, в прибрежных районах Австралии до 5,0-10-6 %. Содержание золота в осадочных породах относительно невелико (1,79-4,57-10 -7 %). В то же время с осадочными формациями связано формирование промышленных скоплений (золотых россыпей). В магматических породах среднее содержание золота соответствует значению 3,57 — 10 -7 %, с тенденцией увеличения среднего содержания золота от кислых пород к щелочным.
Подвижность золота в геологических процессах в основном связана с взаимодействием водных растворов. Наиболее вероятно появление золота в гидротермальных растворах в виде различных простых и смешанных моноядерных комплексов Au+1. К ним относятся гидроксильные, гидроксихлоридные и гидросульфидные комплексы. При более высоких содержаниях сурьмы и мышьяка могут образовываться гетероядерные комплексы золота с этими элементами. Возможен перенос золота в атомарной форме. В низкотемпературных гидротермальных условиях и в поверхностных водах золото мигрирует в виде растворимых металлоорганических комплексов, среди которых наиболее вероятны фульватные и гуматные комплексы. В гипергенных условиях миграция золота происходит в виде коллоидных растворов и механических суспензий. Золото характеризуется рядом факторов, приводящих к его концентрации и фиксации. Наряду с изменением температуры, давления и значения pH, большую роль в концентрации золота играет изменение окислительно-восстановительного потенциала среды. В процессах концентрации золота важную роль играют соосаждение и сорбция.
Читайте далее:



