Недостатком этой реакции является то, что материалы должны быть нагреты как минимум до 200°C, что затрудняет получение золота.
Для этой реакции также можно использовать хлорную воду, которая получается при хлорировании воды:

С какими веществами реагирует золото и каковы его свойства?
Что реагирует с золотом и какие вещества могут определить этот металл в обычных условиях или в лаборатории? Это сложный вопрос, так как в основном это элемент из периодической таблицы и характеризуется инертностью.

Инертность — это способность вещества не реагировать на кислоты, основания и не окисляться при контакте с воздухом и водой. В таблице металл обозначается символом Au, а ‘золото’ в переводе с латинского означает ‘восход солнца’. Золото и платина стали известны как драгоценные металлы только после того, как была обнаружена их способность не реагировать на внешние агенты и химические реагенты. Но химия, как и любая другая наука, не стоит на месте, и было открыто несколько веществ, реагирующих с Au.
Свойства металла
Химические свойства золота указывают на то, что металл может реагировать с некоторыми веществами.
Так с чем же реагирует Au и при каких условиях?
- Ртуть может образовывать с золотом особое соединение, называемое амальгамой. Это сплав двух металлов; молекулы ртути притягивают молекулы Au друг к другу, в результате чего образуется соединение.
- Золото растворяется в aqua regia, что давно известно, но смесь высоких концентраций азотной и соляной кислот не имеет аналогов. Химики используют ее и сегодня, не найдя достойной замены aqua regia, и используют ее в аффинаже.
- Реакция селеновой кислоты и Au начинается только при нагревании концентрированной кислоты до определенной температуры.
- Драгоценный металл также реагирует с йодистым калием. Но в некоторых случаях для идентификации используется простой спиртовой раствор йода, который есть в аптечке первой помощи.
- Жидкий бром и цианистая вода — два других химических вещества, которые могут реагировать с Au.
Способность ртути притягивать молекулы Au известна давно. В прежние времена это свойство металла использовалось для добычи золота. Создавались специальные шлюзы, поверхность которых покрывалась слоем ртути, которая притягивала Au и позволяла увеличить его извлечение. Недостатком этого метода считалась токсичность; человек, постоянно контактирующий с ртутью, жертвовал своим здоровьем во время золотодобычи.
Амальгама является обратимым состоянием; для восстановления первоначальной формы смесь необходимо нагреть примерно до 800 градусов.
Задолго до того, как Дмитрий Менделеев придумал свою периодическую таблицу, алхимики знали о способности золота растворяться в смеси двух кислот. Они смешивали азотную и соляную кислоты и использовали их для различных экспериментов. Ученые того времени кодировали свои записи, поэтому они не записывали реакции, а рисовали их.
Кислотные реагенты
Все кислотные реактивы имеют одинаковый эффект: они оставляют яркое пятно на металле образца, для которого предназначены, или не реагируют вообще. Они также не реагируют на металл более высокой пробы и оставляют коричневое пятно, если проба меньше той, для которой предназначен реактив. Они используются при его приготовлении:
Для различных проб золота готовят растворы в таких пропорциях:
| Проба | Азотная кислота | Соляная кислота | Вода |
|---|---|---|---|
| 375 | 0.595 | 0.405 | |
| 500 | 1 | ||
| 583/585 | 0.46 | 4 капли | 0.54 |
| 750 | 0.593 | 0.011 | 0.396 |
| 833 | 0.687 | 0.013 | 0.3 |
| 900 | 0.692 | 0.013 | 0.295 |
| 958 | 0.787 | 0.02 | 0.193 |
Кислотный реактив для золота 500 пробы можно также считать универсальным реактивом для любого типа золота. Это чистая азотная кислота, которая будет реагировать со всеми типами золота ниже 583 пробы и является самой дешевой и легкодоступной. Все сплавы, содержащие менее половины золота, будут показывать пузырьки под каплей. Чем ниже проба, тем интенсивнее выделение.
Если золота нет вообще, реакция будет мгновенной, появится зеленая пена, сопровождаемая шипением. На серебре низкой пробы она оставит сероватое пятно, а на серебре ниже 800 реакция будет такой же, с образованием пузырьков. На серебре ниже 600 азотная кислота будет кипеть. Ее часто используют в качестве исходного реагента для приблизительного определения металла.
Хлорированное золото
Хлорированное золото часто используется для маркировки предметов, проба и состав которых неизвестны. Оно наиболее эффективно, когда необходимо выявить подделку, например, когда предмет покрыт только слоем золота или вообще не покрыт золотом. Этот реагент используется, если необходимо проверить золото проб 500 и 583/585.
Реагент хлорид золота используется не только для определения золота, он также может применяться для определения других видов драгоценных металлов и сплавов. Для проведения такого анализа каплю реактива наносят на поверхность исследуемого металла и ждут. Через некоторое время образуется пятно определенного цвета, по которому и определяют драгоценный металл, с которым имеют дело.
| Цвет металла | Цвет пятна | Время реакции | Проверяемый металл |
|---|---|---|---|
| Белый | Темно-зеленый | До 2 сек. | Серебро высокой чистоты |
| От желтого до темно-желтого, сопровождается выделением газа | До 2 сек. | Алюминий | |
| Черный | Приблизительно полминуты | Олово | |
| Серовато-белый | Без эффекта | 30-40 секунд | Платина |
| Желтый, быстро становится очень темным | До 2 сек. | Цинк | |
| Сине-белый | Грязно-желтый | До 2 сек. | Свинец |
| Желтый | Без эффекта | До 2 сек. | Высококачественное золото, сплавленное с серебром |
| Каштан | До 6 мин. | Низкокачественные сплавы золота/серебра/меди | |
| Черный | До 2 сек. | Латунь | |
| Бледно-желтый | Черный | До 2 сек. | Низкая концентрация серебра, меди в лигатуре |
| Красный | Нет эффекта | До 2 сек. | Высокая концентрация золота. Медь в лигатуре. |
| Золотой цвет | До 6 минут | Золото низкой чистоты, легированное медью | |
| Черный | До 2 сек. | Медь |
Золото (Au)
Золото — один из самых замечательных металлов, известных человеку с древнейших времен, поскольку наши предки использовали его в религиозных или культурных целях и как одно из самых надежных платежных средств.
В природе золото встречается чаще всего в виде самородков. С некоторыми металлами оно может образовывать природные твердые растворы:
В виде соединений золото встречается в природе гораздо реже (калагерит AuTe2, ауростибит AuSb2). Довольно много золота содержится в морской воде, но добыча такого золота нерентабельна.
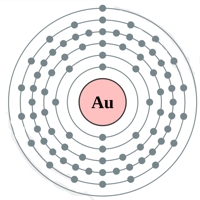
Рис. Структура атома золота.
Электронная конфигурация атома золота — 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 6 4d 10 4f 14 5s 2 5p 6 5d 10 6s 1 (см. Электронное строение атомов). Золото является одним из самых неактивных химических элементов — оно не окисляется на воздухе даже в присутствии влаги, не взаимодействует непосредственно с кислородом, водородом, азотом, углеродом и фосфором.
- золотистый, желтый металл;
- очень пластичный и мягкий — его можно раскатать в прозрачную пленку толщиной в несколько микрон (сусальное золото), которую можно использовать для покрытия различных художественных и религиозных предметов (золочение), придавая им эстетику, которая сохраняется надолго;
- обладает хорошей электро- и теплопроводностью.
- При нагревании вступает в реакцию с галогенами: 2Au + 3Cl2 = 2AuCl3;
- Нерастворим в щелочных и кислотных растворах;
- Растворим в смесях кислот: HCl + HNO3 (aqua regia) и H2SO4+HNO3Au + 3HNO3 + 3HCl = AuCl3 + 3NO2 + 3H2O;
- Металл золото растворяется в виде комплексной соли в водных растворах цианида калия и натрия в присутствии окислителей: 4Au + 8KCN + 2H2O + O2 = 4K[Au(CN)2] + 4KOH;
- легко растворяется в ртути, образуя сплав (амальгаму).
Химия золота

Первая химическая реакция, которая разрушила представление о несокрушимости золота для кислот, — это реакция с aqua regia, основной принцип действия этой кислоты заключается в том, что азотная кислота HNO3 окисляет соляную кислоту, в результате чего образуется чистый хлор, который окисляет несколько драгоценных металлов, включая золото:
Нитрозилхлорид и хлор образуют два активных компонента, которые растворяют золото:
Эта реакция происходит уже при комнатной температуре и может не требовать дополнительного нагрева, в зависимости от тонкости золота.
Из-за высокого содержания хлора и соляной кислоты хлорид золота трижды связывает молекулу хлора с образованием тетрахлороаурата водорода (III) или тетрахлоризолеиновой кислоты.
В результате получается густой желтый порошок, который легко отфильтровать.
И если эта кислота растворяет царское золото, то она была названа в честь растворения царского золота водкой.
Восстановление золота из хлоридов осуществляется путем реакции тетрахлораурат водорода (III) с сульфатом железа (II) FeSO4 , диоксидом серы SO2 , гидразином N2H4 :
Даже перекись водорода ведет себя как восстановитель в реакции восстановления золота:
Взаимодействие чистого углерода с хлоридом золота также приводит к восстановлению золота:
Восстановление золота можно также проводить с хлоридом станола SnCl2 ; эта реакция часто используется в качестве качественной реакции для определения золота, в зависимости от кислотности раствора он становится фиолетово-красным, а при высокой кислотности цвет меняется на более темный.
В качестве качественной реакции для определения золота можно использовать взаимодействие хлорида золота с раствором йодида калия:
Он выпадает в виде нерастворимого темно-зеленого осадка, который, в свою очередь, может быть восстановлен до золота простым нагреванием, причем процесс восстановления начинается при температуре 177 градусов:
Советы по выбору золотых украшений для длительного ношения
Ювелирные изделия, изготовленные из золота разного качества, с использованием различных техник, требуют правильного подхода. Золото 18 карат, серебро 750 пробы менее требовательно к носке. Для тех, кто ведет активный образ жизни, занимается спортом и постоянно носит украшения, рекомендуется выбирать такие высокопрочные сплавы.
Чем меньше добавок в лигатуре, тем лучше она носится и тем меньше требует ухода.
Особые виды золота, такие как белое золото в сложном сплаве или золото с родиевым покрытием и цветное золото, требуют более тщательного и постоянного ухода. Кроме того, необходимо время от времени обновлять покрытие.

Несмотря на инертность самого золота, за золотыми украшениями необходимо тщательно ухаживать.
Добыча золота
Из россыпных месторождений золото может быть извлечено методом флотации (седиментации), который основан на высокой разнице в плотности золота и пустой породы. Золото примерно в 20 раз тяжелее воды и примерно в 8 раз тяжелее песка,
Поэтому золотые зерна можно отделить от песка или от измельченной пустой породы струей воды. Древний метод промывки овечьих шкур, на которых оседали частицы золота, отражен в древнегреческом мифе о золотом руне. Самородки и месторождения золота часто находили вдоль русла рек, которые тысячелетиями размывали золотоносные породы. В древние времена золото добывали только из этих месторождений. Даже сегодня там, где они еще остались, золотоносный песок добывается со дна рек и озер и обогащается в драгах — огромных сооружениях размером с многоэтажный дом, способных перерабатывать миллионы тонн золотоносной породы в год.
Однако этот метод, применявшийся уже в древности, связан с большими потерями. Он уступил место амальгамации (известной уже в первом веке до нашей эры и применявшейся в Америке с XVI века) и цианированию, получившему широкое распространение в Америке, Африке и Австралии в 1890-х годах.
Старый (так называемый ртутный) метод извлечения золота из руды — амальгамация — был основан на том, что ртуть хорошо смачивает золото — как вода смачивает стекло. Мелко измельченную золотую руду встряхивали в бочках с ртутью на дне. Частицы золота прилипали к жидкому металлу, смачивая ртуть со всех сторон. Когда цвет золотых частиц исчезал, золото как бы ‘растворялось’. Затем ртуть отделяли от пустой породы и энергично нагревали. Летучая ртуть удалялась, а золото оставалось неизменным. Недостатками этого метода являются высокая токсичность ртути и неполное извлечение золота: мельчайшие частицы золота плохо смачиваются ртутью.
В конце 19-го и начале 20-го веков основным источником золота стали первичные месторождения. Золотоносная порода дробится и выщелачивается цианидом натрия, который превращает даже самые мелкие частицы в растворимые в воде цианистые соединения. Затем золото извлекается из водного раствора с помощью цинкового порошка: 2Na[Au(CN)2] + Zn → Na[Zn(CN)4] + 2Au. Выщелачивание позволяет извлекать остаточное золото из хвостов заброшенных шахт, эффективно превращая их в новое месторождение. Подземное выщелачивание также является перспективным методом: раствор цианида закачивается в скважину, через трещины попадает в породу, где растворяет золото, а затем раствор откачивается через другие скважины.
Читайте далее:



